
2023年8月17日,同济大学生命科学与技术学院高绍荣和中国农业大学高帅课题组在National Science Review 在线发表了题为 Inhibition of Wnt activity improves peri-implantation development of somatic cell nuclear transfer embryos 的研究论文,该研究发现了导致围着床期克隆胚胎发育失败的表观遗传障碍:Wnt通路的异常激活。更重要的是,通过在培养液中添加Wnt通路抑制剂对Wnt信号通路进行干预抑制(Wnti),可以显著提高克隆胚胎围着床期的发育能力并大幅提高克隆小鼠的出生率。

作为迄今为止唯一一种能使体细胞获得完整全能性的手段,体细胞核移植技术在生物学和再生医学领域具有广阔的应用价值。在过去几十年里,这项技术已在包括灵长类在内的20多种哺乳动物物种上取得了成功,但由于体细胞重构胚胎在重编程过程中存在多种表观遗传的障碍,导致克隆动物极低的出生率并伴随出生胎儿及胎盘的发育缺陷[1]。近年来,许多研究人员尝试通过修正克隆胚胎中异常建立的表观修饰来改善核移植的成功率。同济大学生命科学与技术学院高绍荣及哈佛医学院的张毅等研究团队,通过对核移植胚胎重编程过程中的机制进行研究,鉴定出了在植入前胚胎发育过程中关键的组蛋白修饰(H3K9me3、H3K4me3和H3K9ac)异常所导致的重编程的壁垒,通过有效的干预手段可大幅提升核移植胚胎的植入前发育潜能 [2-5]。另外,核移植胚胎Xist异常激活及H3K27me3依赖性印记基因的表达异常可造成植入后胚胎发育的缺陷 [6, 7]。通过基因编辑技术恢复它们的正常表达水平可提升克隆胚胎植入后发育能力及出生率[6, 8]。
然而,现有的手段在大幅提升核移植技术的囊胚率和植入后发育能力的基础上,其最终的出生率依然远低于正常或体外受精胚胎。这意味着,还有许多其他未知的障碍限制了克隆胚胎发育的能力。回溯整个核移植技术的发展历程,绝大多数研究主要聚焦于植入前和后期克隆胚胎发育异常进行探索。由于缺乏研究的手段和工具,目前对克隆胚胎围着床阶段的发育调控机制知之甚少。
由于围着床期胚胎在母体子宫内生长的不可触及性,严重制约了对克隆胚胎围着床期发育调控机制研究。那么在这一阶段克隆胚胎的形态学发生,信号转导及表观调控事件是如何进行的?为了回答这一问题,高绍荣教授课题组优化建立了3D胚胎培养系统以应用于克隆胚胎的体外培养,这一系统可模拟体内围着床期发育过程,实现了克隆胚胎围着床期发育的可视化。结合体外培养及体内移植实验发现,绝大多数的克隆囊胚在E4.5-E5.25阶段出现发育阻滞,主要表现为内细胞团(inner cell mass,ICM)向外胚层(epiblast, EPI)卵圆桶结构(egg cyclinder)转变时出现明显异常。通过向克隆囊胚中补充同期体外受精胚胎的ICM细胞可极大程度地纠正外胚层形态学转变及胚胎的体内植入率,而补充克隆胚胎的ICM细胞则对围着床期胚胎发育没有改善作用(图1)。
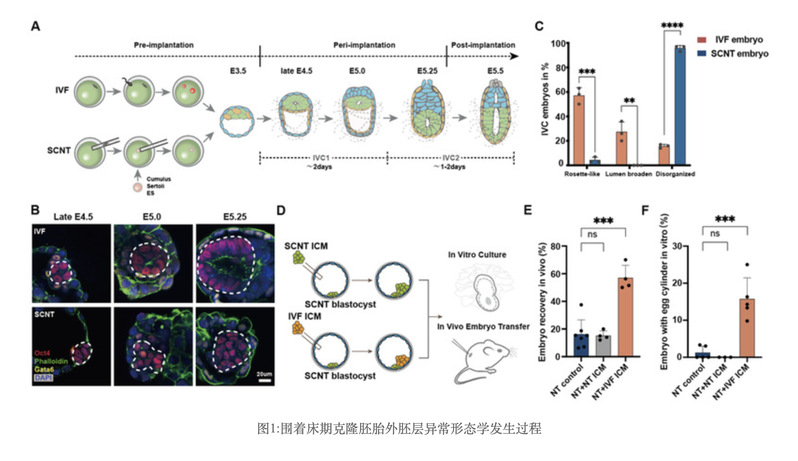
为了验证EPI发育异常的分子机制,研究人员分别对围着床期体外培养的胚胎及体内胚胎进行大量/单细胞转录组分析,结果表明,克隆胚胎的EPI相较于体外受精胚胎,其多能性状态(Naïve-Primed)的转变受阻,并且这种异常现象普遍存在于不同供体细胞(颗粒细胞,支持细胞,胚胎干细胞)来源克隆胚胎的围着床期发育过程。进一步的微量组蛋白ChIP-seq数据分析发现差异表达的多能性基因启动子区分布的H3K27me3重塑也出现异常。
为了寻找多能性转变异常的原因,研究人员分别进行比较转录组、报告系统及信号通路干预等实验,明确了Wnt通路的持续异常激活是阻碍克隆胚胎EPI细胞多能性状态转变的重要障碍。研究人员进一步发现了许多Wnt通路拮抗因子,如Dkk1、Tcf7l1等基因的表达在植入前囊胚阶段即受到显著抑制。通过对小鼠供体细胞和早期胚胎组蛋白修饰的公共数据分析,发现供体细胞中携带的H3K27me3可能是导致着床阶段Dkk1等Wnt通路拮抗基因表达抑制的根源(图2)。
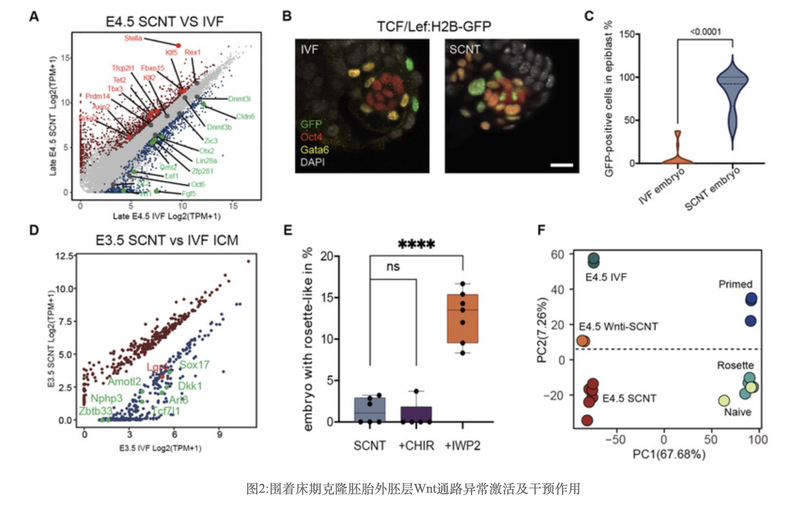
紧接着,为了验证抑制围着床期阶段Wnt通路持续激活对胚胎发育的改善作用,研究人员在培养液中添加了Wnt通路抑制剂IWP2/IWR1-endo对克隆囊胚进行干预,发现Wnt通路抑制剂可显著促进克隆胚胎围着床期的谱系发育轨迹、EPI形态学发生、表观状态及多能性状态的转变(图3)。重要的是,Wnt通路抑制剂处理的克隆囊胚在子宫移植后,可显著提升胚胎着床能力以及出生率(颗粒细胞供体的核移植胚胎出生率从0.72%提高到5.55-7.04%;支持细胞供体的核移植胚胎出生率从0%提高到10.3%)。最后,研究人员通过联合使用过去已报道的重要表观修复手段,发现联合Xist KO和Dnmt3a/b干扰可进一步将核移植囊胚的出生率提升至20%以上。
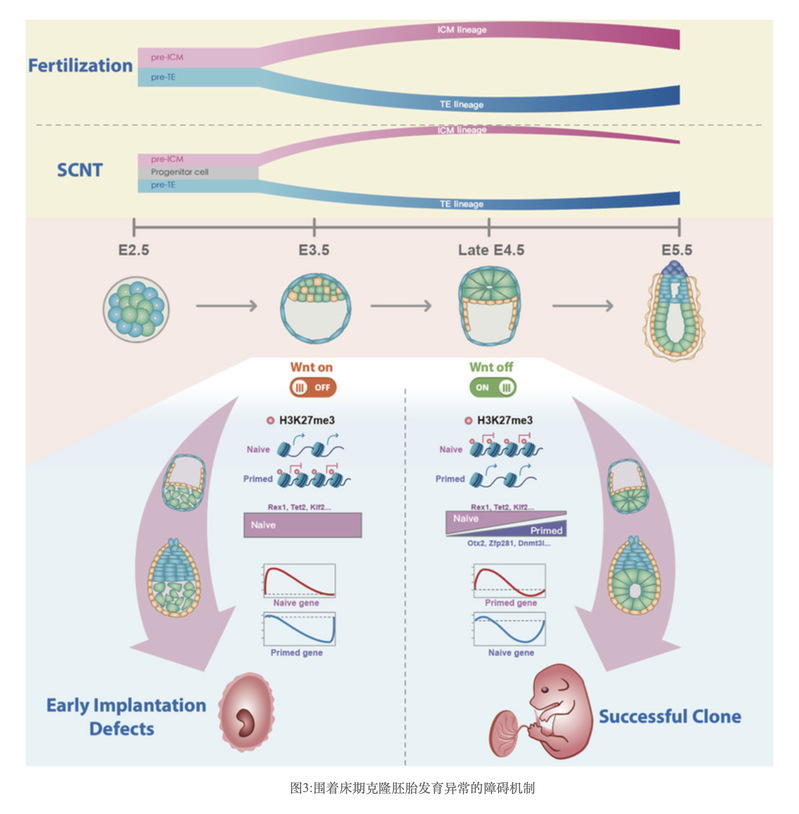
综上所述,该研究利用优化的囊胚模拟着床培养系统首次揭开了克隆胚胎围着床期的动态发育过程,揭示了该时期外胚层形态学发生及多能性转变异常的生物学事件。重要的是,研究人员发现了Wnt通路的持续激活是影响克隆胚胎围着床期发育的一个重要障碍,通过小分子抑制剂干预Wnt激活及联用其他表观修复手段能进一步提升核移植效率。本项研究为理解围着床期胚胎发育,拓展克隆技术在发育生物学、再生医学及畜牧繁殖业的应用提供了重要的理论依据。
本研究的第一作者是同济大学李延鹤博士和北京基因组研究所郑彩宏副研究员。同济大学生命科学与技术学院高绍荣教授、刘文强教授和中国农业大学高帅教授为共同通讯作者。该研究得到了科技部、国家自然科学基金委、及上海市科委等项目的支持。
参考文献
1.Matoba, S. and Y. Zhang, Somatic Cell Nuclear Transfer Reprogramming: Mechanisms and Applications. Cell Stem Cell, 2018.
2.Liu, W., et al., Identification of key factors conquering developmental arrest of somatic cell cloned embryos by combining embryo biopsy and single-cell sequencing. Cell Discov, 2016. 2: p. 16010.
3.Matoba, S., et al., Embryonic development following somatic cell nuclear transfer impeded by persisting histone methylation. Cell, 2014. 159(4): p. 884-95.
4.Yang, G., et al., Dux-Mediated Corrections of Aberrant H3K9ac during 2-Cell Genome Activation Optimize Efficiency of Somatic Cell Nuclear Transfer. Cell Stem Cell, 2020.
5.Gao, R., et al., Inhibition of Aberrant DNA Re-methylation Improves Post-implantation Development of Somatic Cell Nuclear Transfer Embryos. Cell Stem Cell, 2018. 23(3): p. 426-435 e5.
6.Inoue, K., et al., Impeding Xist expression from the active X chromosome improves mouse somatic cell nuclear transfer. Science, 2010. 330(6003): p. 496-9.
7.Matoba, S., et al., Loss of H3K27me3 Imprinting in Somatic Cell Nuclear Transfer Embryos Disrupts Post-Implantation Development. Cell Stem Cell, 2018. 23(3): p. 343-354 e5.
8.Wang, L.Y., et al., Overcoming Intrinsic H3K27me3 Imprinting Barriers Improves Post-implantation Development after Somatic Cell Nuclear Transfer. Cell Stem Cell, 2020. 27(2): p. 315-325 e5.
 |
同济大学高绍荣课题组 地址:上海市四平路1239号同济大学,道交馆 邮编:200092 电话:021-65982276 |